اكتشاف محتمل لعلاج مرض باركنسون باستخدام دواء موجود
هل يوجد علاج محتمل لمرض باركنسون؟ 🤔 قد يكون الجواب نعم! يُشير اكتشاف جديد إلى إمكانية استخدام دواء معتمد من إدارة الغذاء والدواء (FDA) لعلاج السرطان في معالجة هذا المرض العصبي المُتَقدّم.
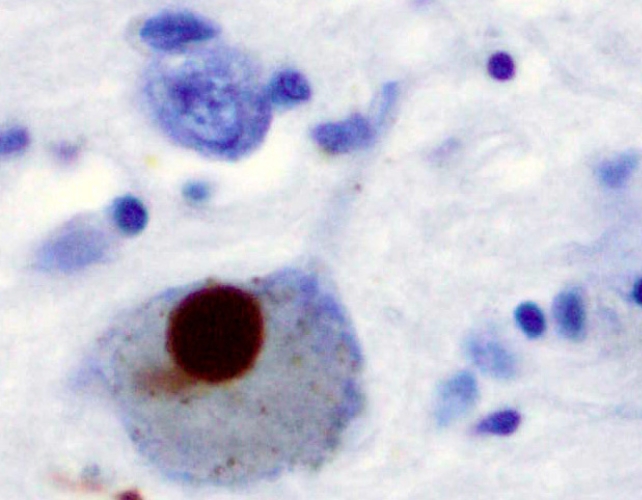
اكتشف الباحثون دور بروتين سطح الخلية Aplp1 في نشر بروتين ألفا-سينوكليين الضارّ في الدماغ، والذي يُعَدّ مُسبّبًا رئيسيًا لمرض باركنسون. ووجدوا أن دواء السرطان Lag3 يُعيق انتشار هذا البروتين الضار في الفئران، مما يُشير إلى إمكانية وجود علاج فعال بالفعل.
في بحثٍ نُشر في العام الماضي، أوضح فريقٌ دولي من العلماء آلية عمل هذين البروتينين معًا في دخول مجموعات البروتين الضارة إلى خلايا الدماغ. يُمكن لهذا الاكتشاف أن يُعيد تشكيل فهمنا لمرض باركنسون وفتح آفاق جديدة لعلاجه.
“بفضل فهمنا الجديد لتفاعل Aplp1 و Lag3، لدينا الآن طريقة جديدة لفهم كيف يساهم بروتين ألفا-سينوكليين في تقدم مرض باركنسون”، يقول عالم الأعصاب شياوبو ماو من جامعة جونز هوبكنز. ويُضيف: “تشير نتائجنا أيضًا إلى أن استهداف هذا التفاعل بالأدوية قد يُبطئ بشكل كبير من تقدم المرض وغيره من الأمراض العصبية التنكسية.”
يُعاني أكثر من ٨.٥ ملايين شخص حول العالم من مرض باركنسون، وهو ثاني أكثر الأمراض العصبية التنكسية شيوعًا بعد مرض الزهايمر. 💔
باعتباره اضطرابًا حركيًا تقدميًا، يُصاحب مرض باركنسون أعراضٌ مثل الرعشة، والصلابة، ومشاكل التوازن، وصعوبات الكلام، وانقطاع النوم، ومشاكل الصحة النفسية. ولكونه غير قابل للشفاء حاليًا، يُصاحب ذلك صعوبة في المشي أو الكلام.
وتُعزى أعراض مرض باركنسون بشكل رئيسي إلى موت خلايا عصبية منتجة للدوبامين في منطقة المادة السوداء في الدماغ، المُسؤولة عن التحكم بالتحركات الدقيقة. يُعتقد أن هذا سببه أجسام لووي، وهي تراكمات غير طبيعية من البروتين تتكون في الغالب من ألفا-سينوكليين مُطوي بشكل خاطئ، وتنتقل بين الخلايا العصبية.
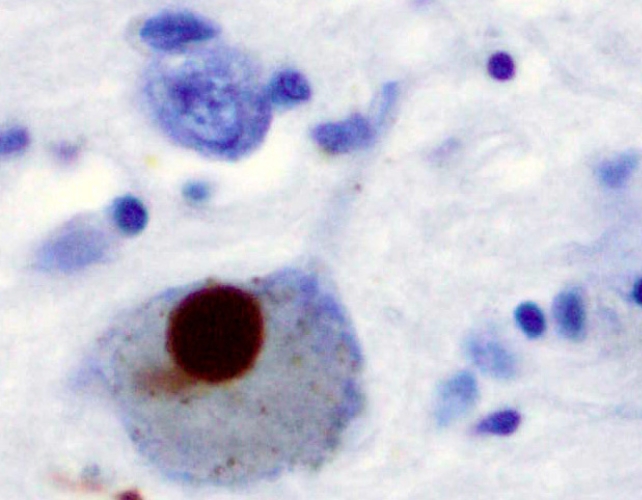
عادةً ما يُحافظ بروتين ألفا-سينوكليين على التواصل الوظيفي بين الخلايا العصبية، لكن المشكلات تنشأ عندما يتغير طيّه ويفقد قابلية الذوبان. هل هو سببٌ لمرض باركنسون أم عرضٌ؟ 🤔 هذا سؤالٌ معقد.
أظهرت الدراسات السابقة على الفئران أن بروتين Lag3 يرتبط ببروتينات ألفا-سينوكليين ويساعد في نشر مرض باركنسون. وعلى الرغم من أن حذف بروتين Lag3 يُعيق هذه العملية بشكل كبير، إلا أنه لا يمنعها تمامًا. يُشير هذا إلى أن بروتينًا آخر مُشاركٌ أيضًا في عملية امتصاص الخلايا العصبية لألفا-سينوكليين ذي الطي الخاطئ.
“أظهرت أبحاثنا السابقة أن بروتين Lag3 ليس البروتين السطحي الوحيد الذي يساعد الخلايا العصبية على امتصاص ألفا-سينوكليين، لذا اتجهنا إلى بروتين Aplp1 في تجاربنا الأخيرة”، يقول عالم الأعصاب فالينا داوسون من جامعة جونز هوبكنز.
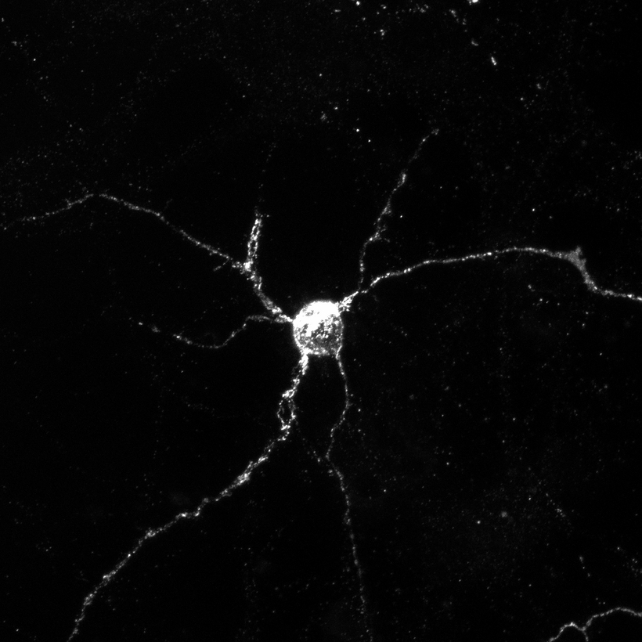
عندما كانت الفئران تفتقر إلى كل من Aplp1 و Lag3، دخل 90% أقل من ألفا-سينوكليين الضار إلى خلايا الدماغ السليمة. هذا يعني أن كمية أكبر من البروتين الضار المتكتل تم حجبها مع غياب كلا البروتينين مقارنةً بحذف بروتين واحد فقط.
أعطى الباحثون فئرانًا طبيعية دواء نڤولوماب/ريلاتليماب، وهو دواء لعلاج سرطان الميلانوما يحتوي على جسم مضاد لـ Lag3. وقد توقف هذا الدواء عن تفاعل Aplp1 و Lag3، مما أدى إلى حجب تكوين مجموعات ألفا-سينوكليين المسببة للأمراض تقريبًا تمامًا.
“كان الجسم المضاد لمُعاكِسة Lag3 ناجحًا في منع المزيد من انتشار بذور ألفا-سينوكليين في نماذج الفئران، وأظهر فعالية أفضل من استنزاف Lag3 بسبب الارتباط الوثيق لـ Aplp1 مع Lag3″، يقول تيد دوسون، عالم الأعصاب بجامعة جونز هوبكنز.
ستكون الخطوة التالية هي اختبار هذا الجسم المضاد على نماذج فئران مرض باركنسون والزهايمر أيضًا. هل سنشهد ثورةً في علاج هذا المرض المُعَقّد قريبًا؟ 🤞
نُشرت الأبحاث في مجلة Nature Communications.
المصدر: رابط المقال الأصلي